70950-160高盐核酸酶用途
关键词: 70950-160高盐核酸酶用途 高盐核酸酶

 2025.12.05
2025.12.05
文章来源:
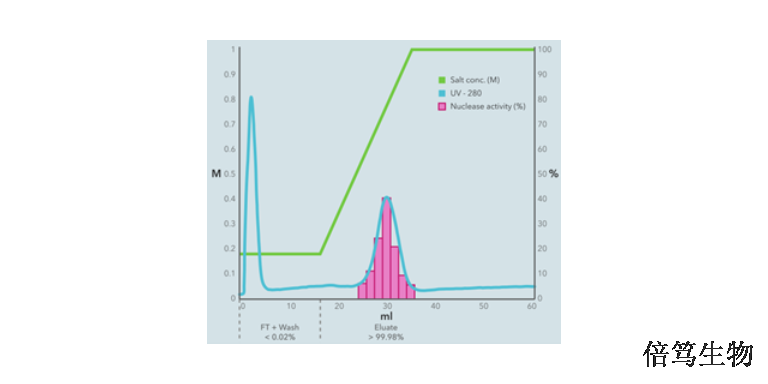
在生物工艺流程中,需要使用核酸酶去除终产品中的核酸污染,而核酸酶作为外源成份,也需要在生产流程中去除。核酸酶去除工艺包括热灭活法、酶抑制剂、离子交换和亲合层析法等。AAV衣壳亚种之间因表面电荷的差异导致不同的的等电点,——空衣壳pI在6.3左右,包装了完整基因组DNA后的病毒颗粒pI大致为5.9。而来自于S.marcescens的全能核酸酶pI 6.85左右,SAN HQ高盐核酸酶pI 9.6左右。因此,在同样的条件下,从AAV溶液中去除SAN HQ高盐核酸酶比去除Benzonase全能核酸酶更容易、更彻底。江西高盐核酸酶售后服务哪家好呢,欢迎咨询上海倍笃生物 。70950-160高盐核酸酶用途
有研究发现,杆状病毒表达载体体系BEV生产的rAAV发生了与293生产体系不同的衣壳蛋白翻译后修饰(post-translationalmodifications,PTMs)。这一差异是否会影响载体趋向性和转导效率还需要进一步验证。除此之外,杆状病毒多重infection会导致载体蛋白VP1、VP2和VP3比例不一致。尽管如此,BEV/Sf9系统仍然是一种颇有吸引力的大规模临床级载体生产策略。随着以后对基因药物需求的增加,AAV载体的需求量也会与日俱增,而BEV系统能够降低AAV的成本,未来还是很有发展潜力的。莱芜区高盐核酸酶厂家电话SAN HQ终产品经过0.22 µm过滤除菌;
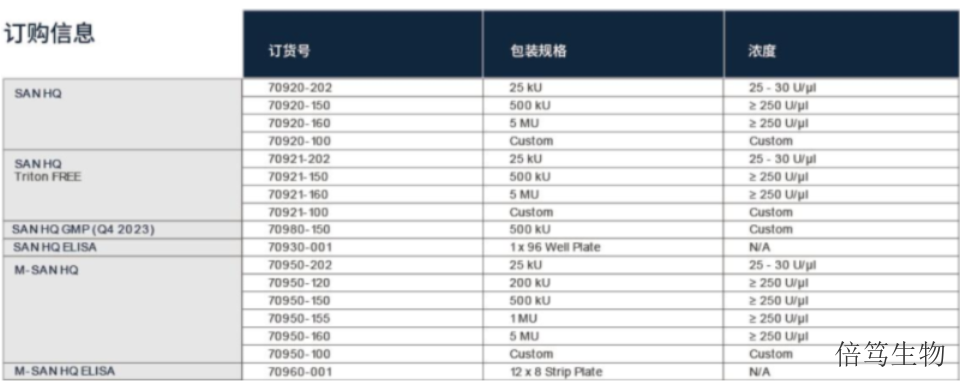
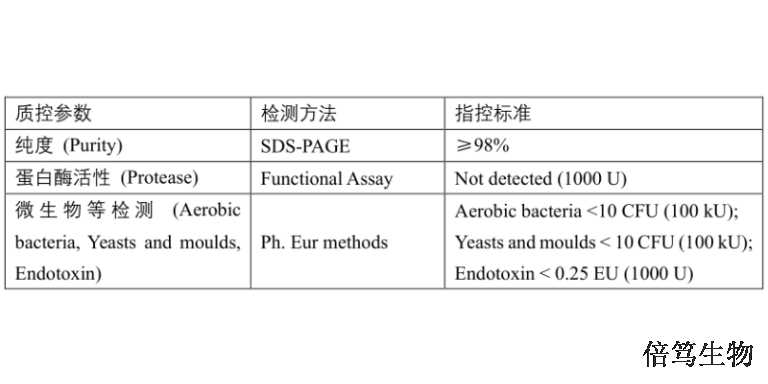
ArcticZymes厂家对盐活性核酸酶系列产品(Salt Active Nucleases,SANs)的生产及质控,在符合ISO13485:2016体系基础上,增加了cGMP质控标准,如microbes、endotoxin、蛋白酶等,符合USP-EP要求。厂家提供HQ级别和GMP级别的SAN HQ高盐核酸酶和M-SAN HQ中盐核酸酶,从成本角度分别满足临床前和早期临床阶段、商业化大规模生产阶段的需求;且GMP级SAN HQ高盐核酸酶已完成在FDA的药物主文件(Drug Master File, DMF)申报备案,助力加快药物申报流程。
ArcticZymes Technologies推出了SAN HQ高盐核酸酶和M-SAN HQ中盐核酸酶,为生物工艺领域提供了革新性、更高效的方案来解决大规模生产中核酸残留问题。此前,受限于盐浓度和核酸酶活性的负调控效应,行业在核酸残留去除效果和酶成本之间寻找平衡,更多的是让工艺选择适应酶。此后,行业可以根据工艺具体需求而选择更合适的酶产品,既能达到理想的去除效果,又能轻松控制酶用量及综合成本,真正实现让酶适应工艺选择。SAN HQ和M-SAN HQ为行业提供更高效率的解决方案。常州高盐核酸酶产品质量哪家好呢,欢迎咨询上海倍笃生物 。

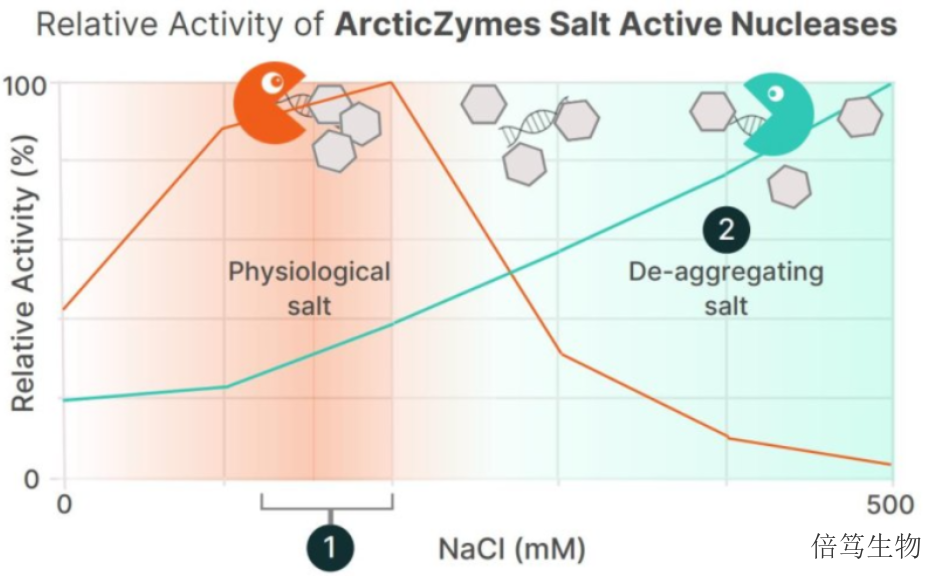
一般来说,生物生产工艺用的核酸酶以BenzonaseTM(BenzonaseTM是Merck的注册商标)为主,能高效降解任何形式(双链、单链、线状、环状)的DNA和RNA。该酶来自于大自然界普遍存在的S.Marcescen,通过E.coli发酵生产得到。该酶的适宜反应条件是低盐浓度范围(<100mM盐浓度),且酶活随着盐浓度上升而下降,在300mM盐浓度时酶活几乎丧失。对于细胞基因药物常用的两种病毒载体LV和AAV,LV由于含有脂包膜结构一般都在生理盐条件下存在,而AAV在高盐条件下不易团聚、更稳定。而在生理盐浓度及更高浓度条件下,Benzonase活性受到抑制。衢州高盐核酸酶服务哪家好呢,欢迎咨询上海倍笃生物 。浙江70921-160高盐核酸酶
SAN HQ高盐核酸酶有两个级别,分别是生物工艺级别SAN HQ和GMP级别SAN HQ GMP。70950-160高盐核酸酶用途
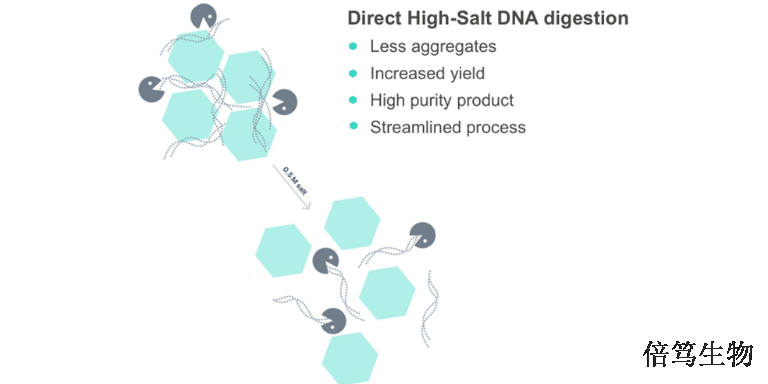
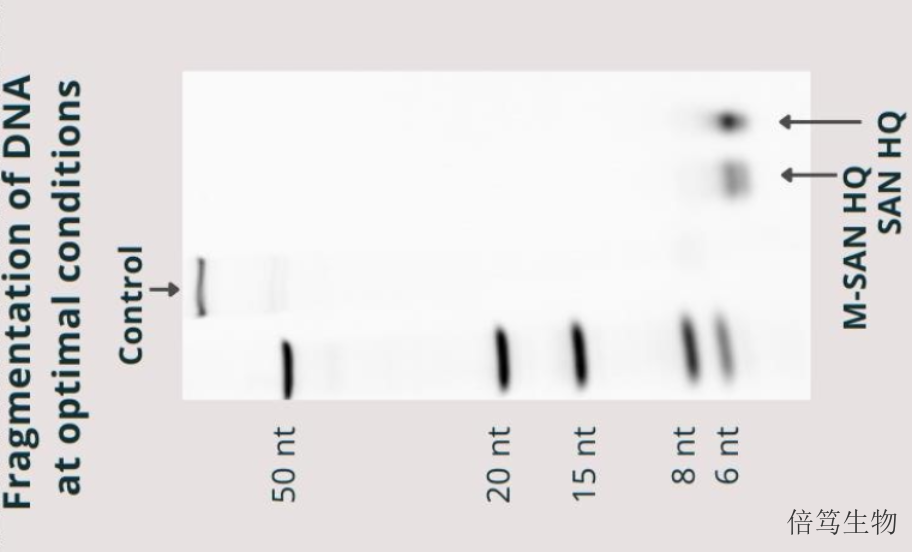
已有文献表明,高盐浓度能够破坏染色质结构,让核小体解聚。在能耐受高盐条件的病毒载体(如AdV/AAV等)生产中,高盐浓度使宿主细胞DNA(HCD)解聚,让核酸片段暴露,提高了核酸片段的可及性。而ArcticZymes的SAN HQ高盐核酸酶能够在高盐条件下更好发挥酶切活性,作为高盐条件下去除HCD的更好选择。SAN HQ高盐核酸酶的出现,让一些通过常规方法很难解决的工艺问题得到高效解决,不仅提高了生产效率,降低了药物生产成本,更拓宽了生物工艺生产的边界。70950-160高盐核酸酶用途

- 吉林70930-001高盐核酸酶 2025-12-04
- 徐州SAN HQ高盐核酸酶厂家 2025-12-04
- 常州SAN HQ高盐核酸酶供应商 2025-12-04
- 宁波70921-202高盐核酸酶供应商 2025-12-04
- 常州70921-160高盐核酸酶供应商 2025-12-04
- 辽宁高盐核酸酶销售电话 2025-12-04
- 浙江特色中盐核酸酶联系方式 2025-12-03
- 河北70921-160高盐核酸酶厂家直销 2025-12-03



- 01 云南哪个公司仪器多面部项目仪器有哪些
- 02 有什么手术无影灯性价比
- 03 潮州养生茶
- 04 贵州5混1病毒采样管生产厂家
- 05 黍峰生物传送式植物表型平台费用
- 06 浙江包含什么医用吊塔成交价
- 07 术中检测肌电图证书
- 08 浙江驼背矫正器支具销售电话
- 09 济宁磷酸胆碱涂层价格
- 10 温州奥托博克智能假肢订制价格