江苏CDE eCTD销售电话
关键词: 江苏CDE eCTD销售电话 eCTD

 2025.12.19
2025.12.19
文章来源:
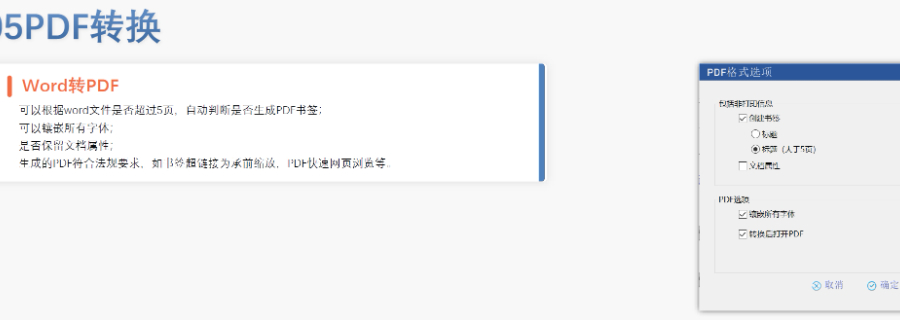
eCTD即是电子化的CTD注册申报方式,相对于传统的纸质递交,eCTD电子递交更便捷、更安全。对于申请者来说,一个产品如在多个市场递交,M2-M5的资料可以共享,极大降低了成本并提高了效率;对审评者来说,eCTD资料的审阅、管理、传输以及归档十分便捷,eCTD格式同时也利于各个地区的yao监部门的审评意见交流。eCTD递交自2003年开始实施以来,以其在创建、传输、复制、审阅、检索、存档以及文件生命周期管理等方面的优势当之无愧地成为全球YAO品注册申报的大势所趋,除了传统的美国、日本和欧盟等ICH成员国之外,加拿大、瑞士、沙特阿拉伯、南非、澳大利亚、新西兰、泰国、新加坡、韩国等地区都已经部分采纳或者正在逐步转向eCTD递交。赋悦科技,做为国内自主研发服务器版eCTDYAO品注册申报软件,让法规注册事务从系统上极大缩短申报周期,助力企业加快产品上市速度。迅速实施,上手简单,项目管理,超链接管理,权限管理,审计追踪;网页登录,异地办公,多人协同,eCTD文件导入,PDF批量一键修复。同时提供短期租赁服务,在保证合规的前提下,为企业降本增效。 美国ANDA注册申报相关技术支持。江苏CDE eCTD销售电话
紧急申报与特殊通道:FDA设置紧急申报通道(如Pre-EUA和EUA),允许在公共卫生事件中快su提交资料。此类申请需在模块,并通过ESG加急处理。eCTD版本兼容性与过渡策略:eCTD,允许。企业需在2024年前完成系统升级,确保XML到HL7RPS的格式转换。过渡期间需同时维护旧版本系统。区域差异与全球化协调:美国模块1要求严格,如UUID标识符和组合申请支持,而欧盟侧重文件引用合规性。FDA与PMDA、EMA通过ICH框架协调eCTD标准,但区域特殊性仍需针对性适配。行业影响与长期价值:eCTD不是技术升级,更是全球yao品监管一体化的驱动力。其标准化、可追溯性和效率提升,推动了跨国多中心试验的协同申报,加速创yao上市进程。 浦东新区国产eCTD软件欧盟eCTD注册外包相关技术支持。
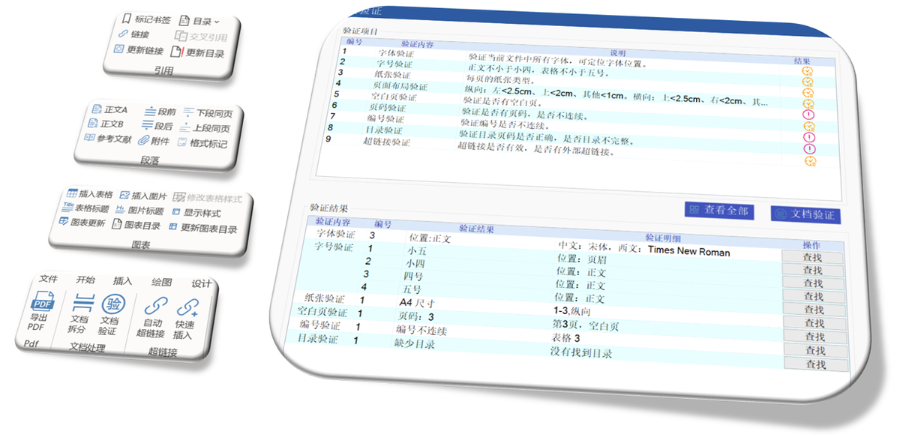
电子递交的合规性与FENG险管理欧盟要求申请人确保电子资料与纸质版本完全一致,若未在规定时间提交纸质文件可能导致注册终止。验证过程中,“错误”级别问题(如文件命名不规范、XML逻辑错误)必须修正,而“警告”和“提示信息”则建议优化以提升审评体验。EDQM和EMA均提供验证工具,申请人需在递交前完成内部预验证。G方费用结构与支付流程欧盟eCTD递交费用因审评程序类型而异:集中程序费用较高,涵盖科学评估和合规审查成本;G家程序费用由各成员国自行设定。CEP申请需向EDQM支付评审费,具体金额根据原料YAO类型和变更复杂度分级。缴费需通过G方指定渠道完成,并附上付款凭证作为模块1的组成部分。多语言支持与翻译要求尽管欧盟允许使用英语提交,但部分成员国要求模块一的行政文件翻译为本地语言。临床试验数据库(如SDTM和ADaM)需以英语呈现,同时提供双语标签以支持多国审阅。Z业翻译服务在确保技术术语准确性方面至关重要,尤其针对复杂YAO学和非临床数据。
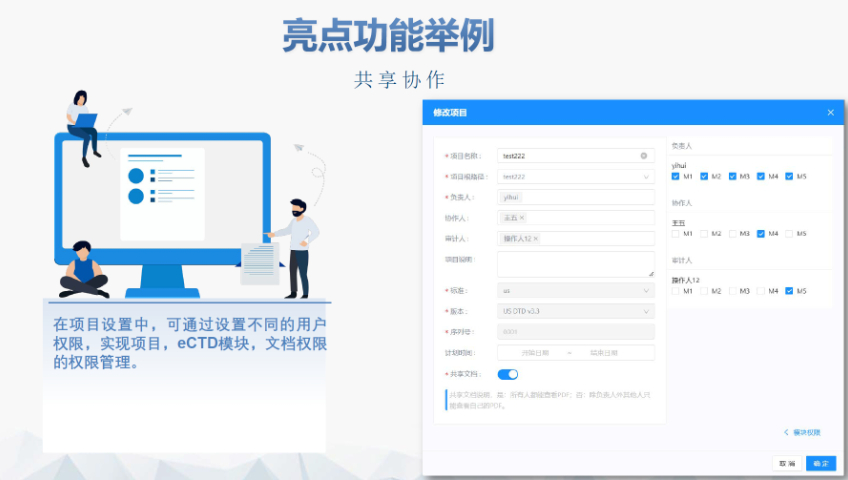
此次eCTD实施范围的扩大对外企而言影响。实施范围的扩大为外企提供了更多选择,特别是在产品线中NDA和AND占比相当的情况下。外企的系统和流程相对成熟,因此它们对eCTD扩大范围持积极态度,更愿意尝试和改变。尽管过程中可能遇到技术或法规上的问题,但企业认为通过不断反馈和与CDE沟通,能够帮助提高整体申报效率和质量。此外,外企还面临向更集成化法规信息管理系统的挑战,特别是当需要迁移到系统时。如果尽早将产品迁移到eCTD,无论是系统迁移还是后续的生命周期管理都会更加顺畅。 随着eCTD实施范围的扩大,供应商将拥有更多的业务机会。然而,中国药品注册体系相对年轻化,在推进eCTD实施过程中可能面临各种问题。短期内,中小企业可能面临资金压力,需要考虑是否投入资金购买的eCTD系统。中长期来看,企业更关注的是如何建立一套完善的文档管理体系,而不是完成递交。这需要企业在前期投入更多时间和精力进行流程优化和人员培训。欧盟IND注册申报相关技术支持。
Z国将进一步与guo际接轨,推进eCTD等标准应用,提高yao品注册效率和质量。AI技术可能在yao品注册领域广泛应用,如辅助审评人员工作。未来yao品注册资料将更注重结构化数据,有助于监管机构gao效获取和利用数据。eCTD等数字化工具将推动yao品监管向智慧监管和全生命周期监管发展,提高监管效率和质量。区块链技术具有应用前景,可构建全球统一的yao品申报数据平台。数据化时代,yao品注册领域将更注重数据收集、分析和利用,为监管机构和企业提供决策支持。总而言之,展望未来,随着eCTD在yao品注册领域的广泛应用和不断发展,Z国将逐步建立起与guo际接轨的yao品注册体系。这将有助于提高z国yao品注册的效率和质量,推动z国yao品走向世界舞台。同时,企业也需要密切关注技术发展动态和监管政策变化,及时调整自身战略和规划,以适应未来的市场竞争和监管要求。 eCTD验证实践手册相关技术支持。黑龙江国内注册eCTD
中IND注册申报相关技术支持。江苏CDE eCTD销售电话
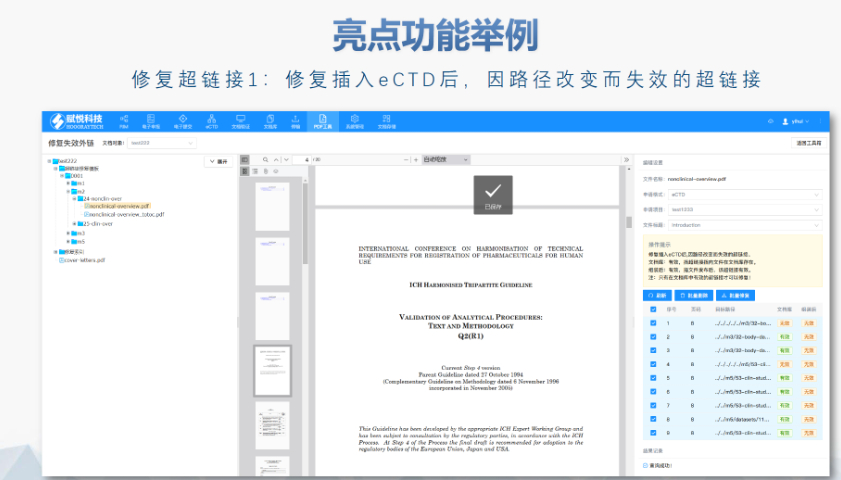
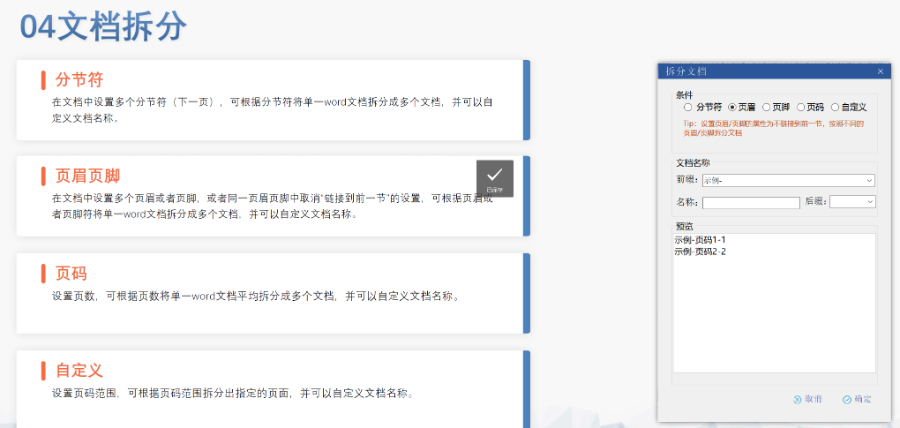
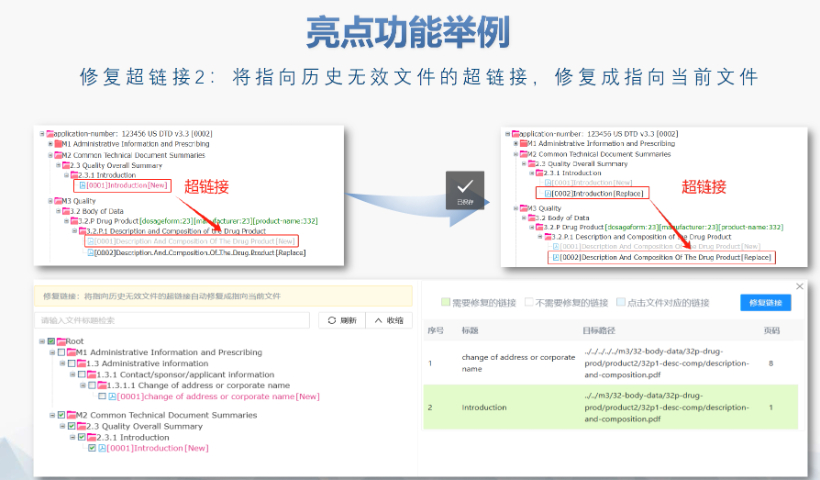
文件生命周期管理:eCTD支持文件替换(Replace)、删除(Delete)等操作,而非增文件。例如,更临床研究方案时需用Replace操作覆盖旧版本。基线提交(BaselineSubmission)可用于补充历史纸质资料,但需在封面函中声明无内容变更。临床数据与研究标签文件(STF):模块4和5中的研究数据需通过STF(StudyTaggingFiles)引用,确保数据与文档关联。FDA要求数据集(如SASXPORT格式)能置于模块3-5,且单个文件超过4GB需拆分。2022年统计显示,58%的ANDA因研究数据技术拒绝标准(TRC)错误被拒。电子签名与表格要求:FDA表格(如356h、1571)需使用数字签名,PDF文件禁止加密或设置编辑限制。电子签名需符合21CFRPart11规范,确保身份验证、不可否认性和数据完整性。外包服务与系统解决方案:赋悦科技累计提交超2000份eCTD申请,外包可降低40%人工错误率。江苏CDE eCTD销售电话

- 浙江ANDAeCTD哪个品牌好 2025-12-18
- 宁波电子申报eCTD哪家好 2025-12-18
- 徐汇区NDAeCTD软件 2025-12-17
- 吴江区赋悦科技eCTD服务电话 2025-12-17
- 浦东新区CDE eCTD注册系统 2025-12-17
- 南京电子申报eCTD名称 2025-12-17
- 山东赋悦科技eCTD找哪家 2025-12-17
- 上海ANDAeCTD递交 2025-12-17



- 01 商超多收银台多对一无线扫描枪厂家
- 02 常州厂房综合布线多少钱
- 03 广东小间距LED屏供应
- 04 佛山无线扫描枪哪个好
- 05 上海碳化硅线晶圆切割刀片
- 06 四川支持多种语言打印的条码打印机型号
- 07 天长定制化开发弱电智能化集成设备
- 08 陕西华为数字人的客户案例分析
- 09 河池监控拼接屏采购
- 10 无锡市水路运输管理系统售价